În medicina veterinară, nu întotdeauna cele mai complexe investigații sunt și cele mai importante în primele momente ale evaluării unui pacient. Uneori, un test simplu, realizat în câteva minute, poate oferi informații importante pentru stabilirea unui diagnostic orientativ și pentru luarea unor decizii rapide.
Microhematocritul este un astfel de test. Deși nu oferă detaliile unei hemoleucograme complete, el are un rol extrem de valoros în evaluarea rapidă și monitorizarea pacienților, în special în situații critice.
Ce este microhematocritul și ce ne arată, de fapt?
Microhematocritul (sau PCV – packed cell volume) reprezintă procentul din sânge ocupat de globulele roșii. Cu alte cuvinte, ne spune cât din volumul total de sânge este format din eritrocite — celulele responsabile de transportul oxigenului.
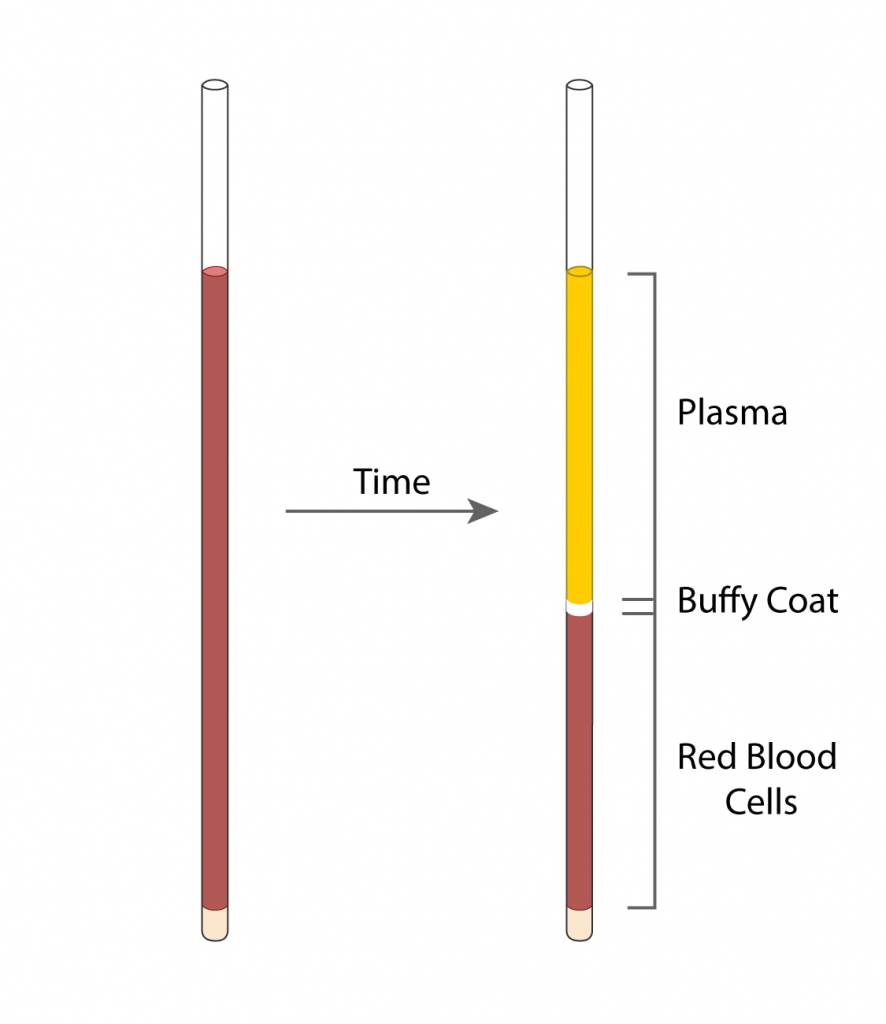
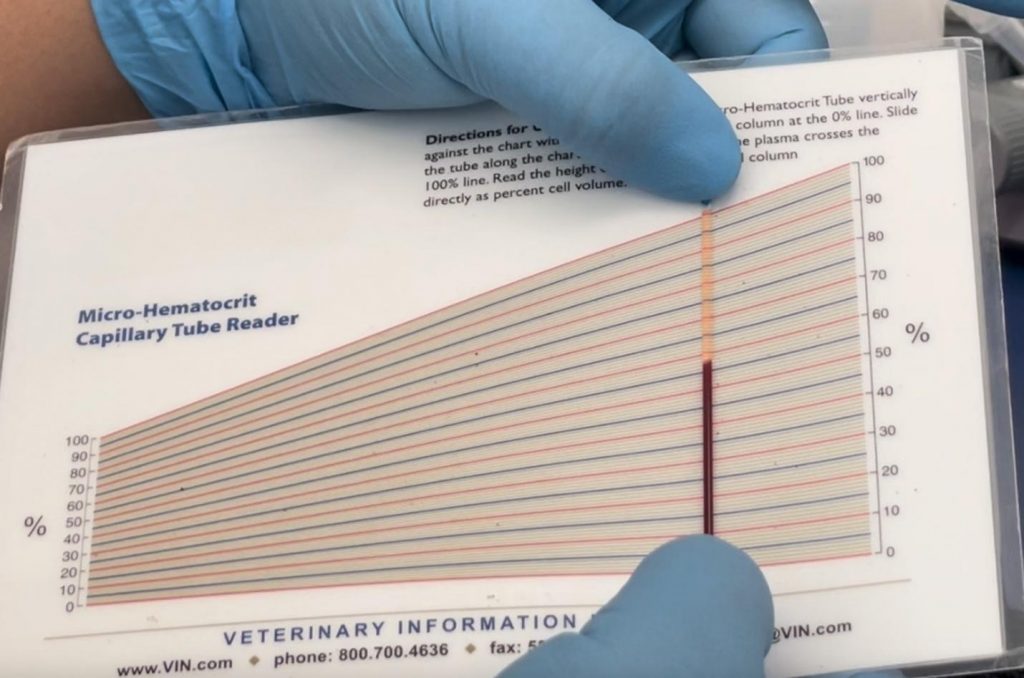
Testul se realizează prin recoltarea unei cantități foarte mici de sânge într-un tub capilar, care este apoi centrifugat. În urma acestui proces, sângele se separă în trei straturi, iar medicul poate măsura proporția ocupată de eritrocite, leucocite și plasmă.
Deși poate părea o analiză simplă și subiectivă, nivelurile acestor trei straturi oferă informații extrem de importante despre starea generală a pacientului.
Importanța în urgențe medicale
În situațiile critice, timpul este limitat. Sunt situații în care medicul veterinar trebuie să ia decizii rapide, uneori înainte de a avea la dispoziție analize complexe.
Microhematocritul are avantajul major că oferă un rezultat în doar câteva minute. Acest lucru permite evaluarea rapidă a unor probleme majore, precum:
- prezența unei anemii severe
- pierderi de sânge (vizibile sau interne)
- gradul de deshidratare
- prezența unei reacții inflamatorii (nivelul mare al leucocitelor)
- prezența icterului sau a hemolizei
De exemplu, un pacient care ajunge în clinică în stare de slăbiciune, colaps sau după un traumatism are nevoie de intervenție imediată pentru stabilizare. În astfel de cazuri, microhematocritul ajută la înțelegerea rapidă a cât de gravă este situația și dacă este necesară o transfuzie sau o stabilizare urgentă.
Informațiile oferite de microhematocrit
Deși nu oferă detalii despre toate tipurile de celule din sânge, microhematocritul poate spune foarte multe atunci când este interpretat corect și în context clinic.
Pe lângă valoarea în sine, medicul poate observa și aspectul plasmei (partea lichidă a sângelui), care oferă indicii suplimentare:
- o culoare roz sau roșiatică poate sugera hemoliză
- o nuanță galben intens poate indica icter
- un aspect tulbure sau lăptos poate sugera niveluri crescute de lipide
Atunci când este asociat cu determinarea proteinelor totale, microhematocritul devine și mai valoros. Împreună, aceste două valori pot ajuta la diferențierea unor situații aparent similare, cum ar fi hemoragia și deshidratarea, care se manifestă asemănător dar se tratează diferit.
Microhematocritul scăzut
O valoare scăzută indică, în general, prezența unei anemii. Aceasta poate avea mai multe cauze:
- pierdere de sânge (hemoragii externe sau interne)
- distrugerea globulelor roșii (anemie hemolitică)
- producție insuficientă la nivelul măduvei osoase
Este important de știut că, în cazul unei hemoragii acute, microhematocritul poate fi inițial normal, deoarece organismul nu a avut încă timp să compenseze pierderea de sânge. De aceea, interpretarea trebuie făcută întotdeauna în context și, deseori, prin repetarea testului. Acesta este un motiv important pentru care se preferă realizarea unui microhematocrit, mai degrabă decât a unei hemoleucograme complete.
Microhematocritul crescut
Cel mai frecvent, o valoare crescută este asociată cu deshidratarea. În această situație, volumul de lichid din sânge scade, iar proporția globulelor roșii pare mai mare.
Alte cauze pot include:
- contracția splenică (de exemplu, în situații de stres)
- policitemia (mai rară)
Interpretarea corectă depinde de corelarea cu alte date, în special cu nivelul proteinelor totale.
Rolul în monitorizarea evoluției
Unul dintre cele mai importante avantaje ale microhematocritului este posibilitatea de a fi repetat frecvent, costul redus făcându-l un instrument perfect de monitorizare. În multe afecțiuni, valorile obținute dintr-o singură hemoleucogramă nu sunt suficiente. Poate fi nevoie de urmărirea în timp a hematocritului pentru a vedea dacă:
- scade în continuare
- se stabilizează
- crește după tratament
Deoarece testul necesită o cantitate foarte mică de sânge și este rapid de realizat, poate fi repetat ori de câte ori este necesar, fără a afecta semnificativ pacientul.
Întrebări frecvent adresate
- Este suficientă realizarea microhematocritului pentru punerea unui diagnostic?
Răspunsul corect este: depinde. Hematocritul este un test de orientare, nu unul complet. El spune cât de gravă este situația și dacă există o problemă majoră legată de globulele roșii sau de volumul de lichide, dar nu identifică cauza exactă. Pentru un diagnostic complet, sunt necesare investigații suplimentare.
Totuși, atunci când consultația este realizată de un medic cu experiență, microhematocritul și contextul clinic al pacientului pot fi suficiente pentru punerea diagnosticului sau pentru inițierea unui diagnostic terapeutic.
- Dacă valorile sunt modificate, care este următorul pas?
Următorii pași depind întotdeauna de contextul clinic. De cele mai multe ori, medicul va recomanda o hemoleucogramă completă pentru a evalua toate liniile celulare, eventual un frotiu sanguin pentru examinare microscopică și, dacă este cazul, analize biochimice sau teste pentru boli infecțioase. În anumite situații, pot fi necesare și investigații imagistice, cum ar fi ecografia, mai ales dacă există suspiciunea unei hemoragii interne.
- De ce microhematocritul și nu hemoleucograma completă?
Alegerea depinde de starea pacientului și de urgența cazului. Microhematocritul este preferat atunci când este nevoie de un răspuns rapid, deoarece poate fi realizat imediat și oferă informații importante în câteva minute. În plus, necesită o cantitate foarte mică de sânge și poate fi repetat frecvent pentru a urmări evoluția pacientului.
Hemoleucograma completă oferă mai multe detalii, dar este utilizată atunci când este nevoie de o evaluare aprofundată, nu neapărat în primele momente ale unei situații critice. Practic, microhematocritul ajută la luarea deciziilor rapide, iar hemoleucograma completează ulterior imaginea dacă este nevoie de clarificări ale cauzelor.
Cel mai important aspect de înțeles este faptul că alegerea anumitor analize nu ține de numărul sau cantitatea lor, ci de relevanța în fiecare context clinic în parte.
- Ce simptome determină alegerea acestui test de laborator?
Microhematocritul este ales în special atunci când simptomele sugerează o urgență. Printre acestea se numără letargia severă, slăbiciunea brusc instalată, colapsul, mucoasele palide, traumatismele sau suspiciunea de hemoragie. De asemenea, este util și în cazurile de deshidratare evidentă. În toate aceste situații, medicul are nevoie de un răspuns rapid pentru a decide următorii pași.
- Ce informații nu oferă microhematocritul?
Microhematocritul nu oferă informații despre:
- numărul și tipul leucocitelor – tipul inflamației
- trombocite – deficitele de coagulare
- cauza exactă a anemiei
De aceea, el nu înlocuiește hemoleucograma completă mereu, ci o completează. Este un instrument de orientare rapidă, dar există situații în care nu oferă un diagnostic complet.
Surse
- Villiers, E., & Ristic, J. (eds.). BSAVA Manual of Canine and Feline Clinical Pathology. British Small Animal Veterinary Association.
- Weiss, D. J., & Wardrop, K. J. (eds.). Schalm’s Veterinary Hematology. Wiley-Blackwell.
- Latimer, K. S. (ed.). Duncan and Prasse’s Veterinary Laboratory Medicine: Clinical Pathology. Wiley-Blackwell.
- Thrall, M. A., Weiser, G., Allison, R. W., & Campbell, T. W. Veterinary Hematology, Clinical Chemistry, and Cytology, 3rd Edition. Wiley-Blackwell
- https://vetgirlontherun.com/wp-content/uploads/2024/08/Featured-Image_Pcv_TP-Video.jpg
- https://humanbiomedia.org/activities/circulatory-system/hematocrit/hematocrit-layer-separation.png